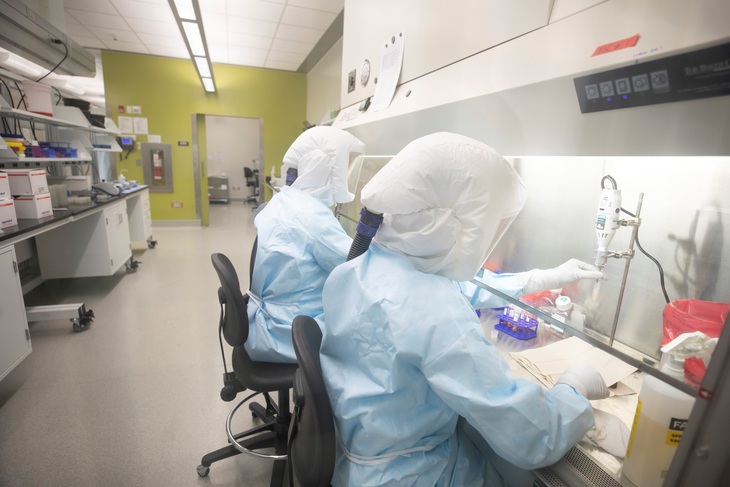
Thế giới sẽ chờ ít nhất một năm để có văcxin đối phó với bệnh viêm phổi cho chủng virus corona mới - Ảnh: REUTERS
Không như những đợt bùng phát dịch Ebola, Zika hay Hội chứng hô hấp Trung Đông (MERS), khi đó việc sản xuất văcxine mất vài năm, Trung Quốc đã nhanh chóng cung cấp mã gen của chủng virus nCoV-2019, giúp các nhà khoa học nhanh chóng bắt tay nghiên cứu nguồn gốc của chủng virus mới, khả năng biến đổi, cũng như cách để đối phó.
Với sự tiến bộ của công nghệ và cam kết hỗ trợ nghiên cứu chống dịch bệnh của các nước, các cơ sở nghiên cứu đã nhanh chóng bắt tay vào hành động.
Tốc độ chưa từng thấy
Tại phòng nghiên cứu của Công ty công nghệ sinh học Inovio ở San Diego, Mỹ, các nhà nghiên cứu đã phát triển loại văcxin có tên INO-4800, dự kiến bắt đầu thử nghiệm trên người vào mùa hè năm nay, theo BBC.
Kate Broderick, lãnh đạo cấp cao phụ trách nghiên cứu và phát triển tại Inovio, cho biết ngay khi Trung Quốc cung cấp mã gen của chủng virus mới, "chúng tôi đã đưa nó qua công nghệ máy tính phòng thí nghiệm và thiết kế ra một loại văcxin trong vòng ba giờ".
"Văcxin ADN của chúng tôi rất mới ở việc chúng sử dụng chuỗi ADN từ virus để nhắm vào các phần cụ thể của mầm bệnh mà chúng tôi cho rằng cơ thể sẽ có phản ứng mạnh mẽ nhất. Sau đó, chúng tôi dùng các tế bào của chính bệnh nhân làm nhà máy sản xuất văcxin, củng cố cơ chế phòng vệ tự nhiên của cơ thể" - bà Broderick giải thích.
Inovio cho biết nếu thử nghiệm ban đầu thành công, họ sẽ tiến hành thử nghiệm lớn hơn vào cuối năm nay.
Chưa biết tình hình dịch viêm phổi do chủng virus nCoV-2019 sẽ diễn biến như thế nào vào cuối năm nay, tuy nhiên Inovio cho biết nếu đi đúng kế hoạch, văcxin của họ sẽ là loại văcxin được phát triển và thử nghiệm nhanh nhất trong tình huống bùng phát dịch.
Trong đợt bùng phát dịch Hội chứng hô hấp cấp tính (SARS) năm 2002, Trung Quốc cung cấp thông tin chậm trễ khiến việc nghiên cứu văcxin bắt đầu khi dịch gần như đã kết thúc.
Các nghiên cứu văcxin nói trên do Liên minh cải tiến sẵn sàng chuẩn bị đối phó đại dịch (CEPI) tài trợ. CEPI được thành lập cách đây ba năm, sau đợt bùng phát dịch Ebola ở châu Phi, và được các tổ chức và chính phủ nhiều nước tài trợ.
"Chúng tôi đang làm việc với tốc độ chưa từng thấy" - tờ Financial Times ngày 30-1 dẫn lời Richard Hatchett, lãnh đạo CEPI, nói.
Nhanh hơn nữa?
CEPI cũng đang tài trợ cho hai chương trình nghiên cứu văcxin chống chủng virus corona mới tại Đại học Queensland, Úc, và chương trình phối hợp giữa Viện các bệnh truyền nhiễm và dị ứng quốc gia (NIAID) Mỹ và Công ty Moderna. NIAID cho biết họ có thể rút ngắn thời gian đưa văcxin ngừa virus nCoV-2019 vào thử nghiệm lâm sàng ở người xuống còn 3 tháng nhờ tiến bộ công nghệ phát triển từ dịch SARS trước đây.
Tại Trung Quốc, Công ty Clover Biopharmaceuticals thậm chí công bố kế hoạch tham vọng hơn là phát triển loại văcxin dựa trên protein của virus corona và có thể đưa vào thử nghiệm trong vài tuần tới. Trung Quốc cũng đang bắt tay với Nga để phát triển văcxin chống chủng virus nCoV-2019.
Tỉ phú giàu nhất Trung Quốc Jack Ma đã tuyên bố tài trợ 100 triệu nhân dân tệ, khoảng 14 triệu USD, trong đó gần một nửa sẽ dành cho việc phát triển văcxin chống virus nCoV-2019.
Tuy nhiên, các nhà khoa học cho rằng dù đẩy mạnh việc phát triển văcxin, việc thử nghiệm và sản xuất sẽ còn đối mặt với nhiều thách thức khác. Do đó, thế giới phải chờ ít nhất một năm nữa mới có thể có được loại văcxin hiệu quả để đối phó với virus nCoV-2019.
















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận