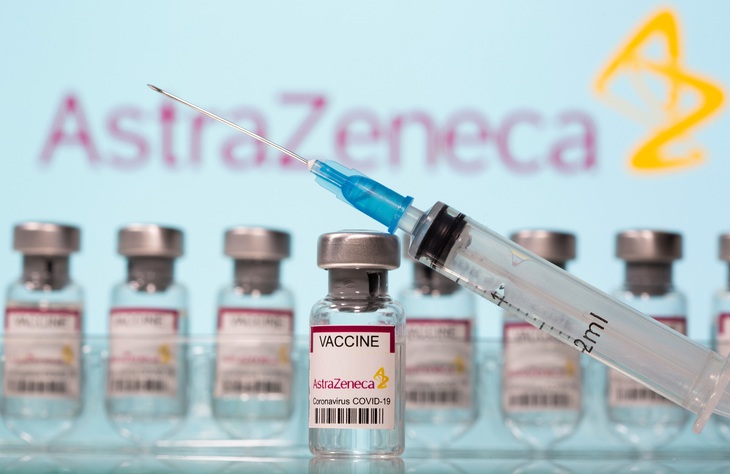
Vắc xin do AstraZeneca và Đại học Oxford (Anh) nghiên cứu, sản xuất chiếm phần lớn trong cơ chế phân phối vắc xin COVAX của Tổ chức Y tế thế giới và từng được gọi là "vắc xin cho thế giới" - Ảnh: REUTERS
"Chúng tôi sẽ ngừng tiêm loại vắc xin này tới khi mọi nghi ngờ được xóa tan. Nếu các chuyên gia không đưa ra được bằng chứng việc tiêm vắc xin an toàn cho dân, Bulgaria sẽ tiếp tục dừng tiêm vắc xin AstraZeneca", Thủ tướng Bulgaria Boyko Borissov nhấn mạnh trong thông cáo chiều tối 12-3 (giờ Việt Nam).
Theo báo New York Times, Đan Mạch đã quyết định ngừng tiêm vắc xin của AstraZeneca trong vòng 2 tuần để làm rõ thông tin những người được tiêm gặp phải tình trạng máu đông. Một phụ nữ 60 tuổi ở Đan Mạch đã chết vì tình trạng máu đông sau khi được tiêm vắc xin của AstraZeneca, làm dấy lên câu hỏi liệu vắc xin có phải là nguyên nhân hay không.
Tình trạng máu đông có thể dẫn tới thuyên tắc phổi hoặc huyết khối tĩnh mạch sâu. Các nhà điều tra và cơ quan y tế châu Âu đã vào cuộc tìm câu trả lời ngay lập tức.
Trong bối cảnh đó, danh sách các nước ngừng tiêm vắc xin AstraZeneca ngày một kéo dài. Na Uy, Iceland và mới nhất là Bulgaria đã quyết định đình chỉ không thời hạn việc tiêm chủng.
Áo, Estonia, Lithuania, Luxembourg và Latvia hôm 11-3 cũng tuyên bố sẽ ngưng tiêm vắc xin AstraZeneca thuộc lô ABV5300. Theo Cơ quan quản lý dược phẩm châu Âu (EMA), lô này có hơn 1 triệu liều, được phân bố cho 17 nước trong Liên minh châu Âu.
Ý cũng ra lệnh ngừng tiêm vắc xin AstraZeneca thuộc lô ABV2856 sau khi ghi nhận "một số vụ việc nghiêm trọng" nhưng không nói rõ chi tiết, theo Đài CNN.
Tác động từ hành động của nhiều nước châu Âu đã bắt đầu xuất hiện trên thế giới. Tại châu Á, Thái Lan đã quyết định ngừng tiêm vắc xin AstraZeneca để bảo đảm an toàn.
"Dù chất lượng của loại vắc xin này là tốt, nhưng vì nhiều nước đã ngừng nên chúng tôi cũng sẽ làm thế", một phát ngôn viên của Chính phủ Thái Lan giãi bày ngày 12-3.
Các quan chức y tế ở những nước kể trên đều khẳng định việc tạm dừng chỉ là biện pháp cần thiết để làm rõ các thông tin, nghi ngờ. Đức và Pháp, hai nước lớn của châu Âu, tuyên bố vẫn sẽ tiếp tục triển khai vắc xin AstraZeneca.
Người đứng đầu chương trình tiêm vắc xin của Pháp, ông Alain Fischer, khẳng định vắc xin ngừa COVID-19 của Hãng AstraZeneca đã cho thấy hiệu quả tốt. Ông này nhấn mạnh trên đài phát thanh rằng Pháp sẽ tiếp tục sử dụng loại vắc xin này trong chiến dịch tiêm chủng.
Hôm 11-3, EMA cũng lên tiếng trấn an và ủng hộ việc tiếp tục sử dụng vắc xin AstraZeneca. Cơ quan này lập luận những lợi ích của loại vắc xin này đem lại vượt trội so với những rủi ro nên vẫn có thể sử dụng.
AstraZeneca nói gì?
Trong tuyên bố ngày 11-3, AstraZeneca cho biết họ không tìm thấy bằng chứng nào về việc tăng nguy cơ thuyên tắc phổi hoặc huyết khối tĩnh mạch sâu sau khi xem xét hơn 10 triệu hồ sơ. Hãng dược có trụ sở tại Thụy Điển cho biết quá trình xem xét còn tính cụ thể đến tuổi tác, giới tính, lô sản xuất và quốc gia sử dụng.
Chính phủ Anh cùng ngày cũng lên tiếng bảo vệ vắc xin của AstraZeneca. "Vắc xin của AstraZeneca vừa an toàn vừa hiệu quả. Nếu bạn được yêu cầu tiêm chủng, hãy tự tin tiêm", một phát ngôn viên của Thủ tướng Anh Boris Johnson khẳng định.


















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận