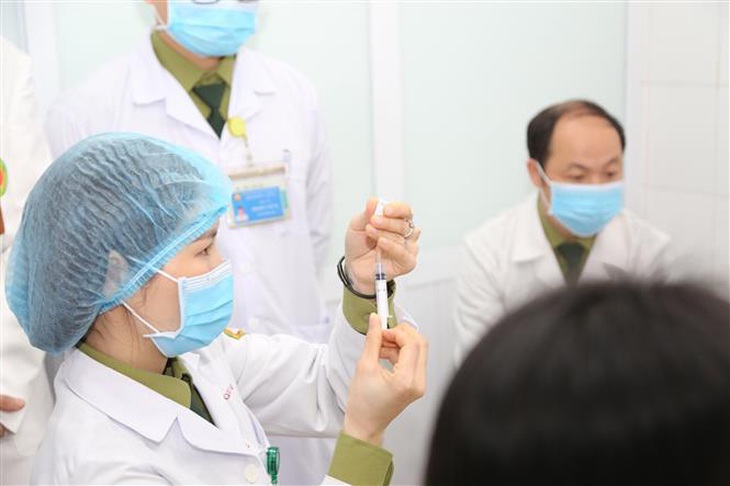
Bác sĩ chuẩn bị tiêm mũi vắc xin ngừa COVID-19 Nano Covax nhóm liều 50mcg cho tình nguyện viên - Ảnh: TTXVN
Theo thông báo vừa được Bộ Y tế gửi tới báo giới, Bộ Y tế cho rằng quy định của Tổ chức Y tế thế giới (WHO) và các nước như Mỹ, châu Âu, Nhật, Hàn Quốc… vắc xin trước khi đưa vào sử dụng khẩn cấp bắt buộc phải thử nghiệm lâm sàng trên người với 3 giai đoạn.
Giai đoạn 3 quan trọng nhất
"Giai đoạn 3 được thực hiện trên quy mô lớn, với mục tiêu đánh giá tính an toàn và hiệu quả bảo vệ của vắc xin. Kết quả của giai đoạn này sẽ quyết định việc vắc xin đó có được phê duyệt để triển khai tiêm chủng rộng rãi hay không.
Kể cả sau khi đã được phê duyệt, các loại vắc xin đó đều phải liên tục bổ sung, cập nhật các thông tin, dữ liệu liên quan đến tính an toàn, hiệu quả trong quá trình sử dụng" - Bộ Y tế cho biết.
Bộ Y tế cho rằng thử nghiệm lâm sàng giai đoạn 1 và 2 được tiến hành ở quy mô nhỏ, trên một số nhóm quần thể để kiểm tra độ an toàn, tính sinh miễn dịch và xác định liều lượng tối ưu. Việc đánh giá tính sinh miễn dịch trong giai đoạn 1 và 2 này không phải là yếu tố quyết định cho việc phê duyệt khẩn cấp.
"Chỉ có kết quả thử nghiệm lâm sàng giai đoạn 3 mới là yếu tố quyết định để đánh giá vắc xin này có hiệu quả bảo vệ hay không, có làm giảm nguy cơ mắc COVID-19 hay không, hoặc giảm nhẹ tình trạng bệnh hay không" - báo cáo cho biết.
"Trong bối cảnh dịch COVID-19 bùng phát rộng trên toàn thế giới, việc cấp phép khẩn cấp cho một loại vắc xin phòng COVID-19 là cần thiết. Tuy nhiên, điều này không có nghĩa là bỏ qua các giai đoạn thử nghiệm lâm sàng bắt buộc" - Bộ Y tế giải thích.
Bộ Y tế cũng cho rằng việc cấp phép khẩn cấp sử dụng vắc xin COVID-19 hiện nay là do điều kiện dịch bệnh nên chưa đủ thời gian để theo dõi được vắc xin trong thời gian dài như thông lệ. Mặc dù vậy, để đảm bảo tính an toàn, vẫn phải thực hiện đầy đủ quy trình đánh giá hiệu quả bảo vệ của vắc xin.
Cũng giống như thông lệ quốc tế, tất cả vắc xin COVID-19 trước khi đưa vào sử dụng khẩn cấp tại Việt Nam đều phải tuân thủ thử nghiệm lâm sàng qua 3 giai đoạn, trên nguyên tắc đảm bảo 3 yếu tố: an toàn, sinh miễn dịch và quan trọng nhất là hiệu quả bảo vệ.
Từ tháng 1-2020 đến nay, Bộ Y tế đã phê duyệt có điều kiện cho 4 loại vắc xin COVID-19: Comirnaty của Pfizer, A2D1222 của AstraZeneca, Sputnik-V của Gamalaya, Vero-Cell của Sinopharm cho nhu cầu cấp bách trong phòng chống dịch COVID. Ngoài ra, vắc xin Moderna cũng đang trong quá trình xem xét phê duyệt.
"Tất cả các vắc xin nói trên đều phải trải qua 3 giai đoạn thử nghiệm lâm sàng. Trong đó, thử nghiệm lâm sàng giai đoạn 3 có quy mô từ 20.000 đến 50.000 người tham gia" - Bộ Y tế cho biết.
Cụ thể theo Bộ Y tế, vắc xin của AstraZeneca thử nghiệm lâm sàng giai đoạn 3 tại 11 quốc gia với 49.626 người tham gia. Vắc xin Vero-Cell của Sinopharm thử nghiệm lâm sàng tại 6 quốc gia với trên 45.000 người.
Vắc xin Sputnik-V thử nghiệm lâm sàng tại 5 quốc gia với 21.977 người, vắc xin của Pfizer thử nghiệm lâm sàng tại 6 quốc gia với 43.418 người và vắc xin của Moderna thử nghiệm tại 4 quốc gia với 30.420 người.
Điều kiện phê duyệt sớm cho vắc xin nội
Thông báo này của Bộ Y tế được phát ra sau khi nhà sản xuất Nano Covax có văn bản đề nghị Thủ tướng sớm cho phép cấp phép khẩn cấp có điều kiện cho vắc xin này. Đây là vắc xin có tiến độ phát triển nhanh nhất trong số 3 vắc xin nội, hiện đang thử nghiệm lâm sàng giai đoạn 3 trên người, với 1.000 người tham gia giai đoạn 3a đã tiêm xong mũi 1 hôm 18-6.
Dự kiến giữa tháng 7, 1.000 người này sẽ hoàn tất tiêm mũi 2, chuyển sang giai đoạn lấy mẫu đánh giá tính an toàn, tính sinh miễn dịch và hiệu quả bảo vệ của vắc xin. Trong thời gian đó sẽ tiếp tục tiêm 12.000 người tham gia thử nghiệm giai đoạn 3 tại nhiều tỉnh thành.
Trả lời Tuổi Trẻ Online cuối tuần trước, lãnh đạo Bộ Y tế cho biết có thể xem xét sớm phê duyệt khẩn cấp có điều kiện vắc xin này, trong bối cảnh dịch bệnh, cụ thể theo nhiều nguồn tin có trách nhiệm là sau khi có kết quả đánh giá hiệu quả vắc xin của giai đoạn 3a, tức là dự kiến vào đầu quý 4 năm nay.
Tuy nhiên ngày 22-6, Cục Khoa học, công nghệ và đào tạo lại cho rằng việc nhà sản xuất đề nghị xem xét cấp phép sớm tới Thủ tướng là "nóng vội", "chưa đủ cơ sở dữ liệu".

















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận