
GS Paolo A.Ascierto làm việc tại Viện nghiên cứu và điều trị ung thư quốc gia - Quỹ Giovanni Pascale ở Napoli (Ý) - Ảnh: TODAY
Chúng ta phải kiên nhẫn và chờ đợi kết quả thử nghiệm. Các dấu hiệu về lợi ích điều trị đang gia tăng nhưng chúng ta chưa có dữ liệu trước vài tuần nữa.
GS Ascierto
Ý cũng có một nhân vật nổi đình nổi đám không kém là GS Paolo A. Ascierto nhưng hành động thận trọng hơn. Ông nung nấu ý tưởng sử dụng thuốc điều trị viêm khớp dạng thấp tocilizumab để điều trị biến chứng viêm phổi nặng nơi bệnh nhân COVID-19.
Thử nghiệm TOCIVID-19 ở Ý
GS Paolo A. Ascierto hiện là giám đốc khoa u ác tính, liệu pháp miễn dịch ung thư và trị liệu sáng tạo tại Viện nghiên cứu và điều trị ung thư quốc gia - Quỹ Giovanni Pascale ở Napoli (thủ phủ vùng Campania).
Trao đổi với kênh truyền hình TgCom24 (Ý), ông giải thích: "Các bác sĩ ung thư chúng tôi biết tocilizumab vì đã sử dụng thuốc đó để giảm tác dụng phụ liên quan đến liệu pháp miễn dịch. Chúng tôi quan sát thấy tocilizumab có phản ứng miễn dịch quan trọng như phản ứng ở phổi nơi người nhiễm virus corona. Từ đó chúng tôi nảy ra ý tưởng sử dụng loại thuốc này để đối phó với đại dịch COVID-19".
Với trực giác nhạy bén trong nghề, GS Ascierto đã liên hệ với đồng nghiệp Trung Quốc để thu thập thêm thông tin vì họ cũng từng thử nghiệm tocilizumab. Các nhà khoa học Trung Quốc đã dùng thuốc tocilizumab trên 21 bệnh nhân COVID-19. Từ 24-48 tiếng sau khi nhận được mũi tiêm một liều duy nhất, các bệnh nhân cải thiện bệnh tình rõ rệt. Sốt giảm nhanh. 15/20 bệnh nhân giảm nhu cầu thở oxy bổ sung (75%) vài ngày sau khi tiêm. Tuy nhiên, kết quả này chỉ mang giá trị tham khảo vì không được các nhà khoa học khác đánh giá.
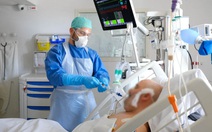
Đầu tháng 3-2020, các bác sĩ ung thư Ý bắt đầu tiêm thuốc tocilizumab cho hai bệnh nhân COVID-19 nằm tại Bệnh viện Cotugno (Napoli). 24 tiếng sau, một bệnh nhân có dấu hiệu cải thiện, không cần đặt nội khí quản nữa trong khi trước đó nhập viện trong tình trạng đặc biệt nguy kịch. Bệnh nhân kia tiến triển tích cực nhưng chậm hơn.
Giữa tháng 3, các nhà khoa học đã khẩn trương gửi quy trình nghiên cứu về sử dụng thuốc tocilizumab trên bệnh nhân COVID-19 cho Cơ quan Quản lý dược phẩm Ý (AIFA) để thẩm định trước khi mở rộng nghiên cứu. AIFA đồng ý tiến hành chương trình thử nghiệm độc lập mang tên TOCIVID-19 (giai đoạn 2) đối với thuốc tocilizumab trong điều trị viêm phổi cho bệnh nhân COVID-19. Thử nghiệm nhằm hai mục tiêu chính: thu thập dữ liệu chất lượng tốt về phương pháp luận và giám sát mọi sử dụng ngoài giấy phép lưu hành (AMA) để đánh giá tác động của thuốc đến tỉ lệ tử vong.
Sau đó, nhiều bệnh viện khác ở Ý đã sử dụng thuốc tocilizumab. Kết quả đạt được rất khả quan. Dù vậy ngày 27-3, GS Ascierto đã kêu gọi trên Facebook cần lạc quan một cách thận trọng: "Chúng ta phải kiên nhẫn và chờ đợi kết quả thử nghiệm. Các dấu hiệu về lợi ích điều trị đang gia tăng nhưng chúng ta chưa có dữ liệu trước vài tuần nữa".
Tocilizumab (tên biệt dược Artemra do Công ty Roche của Thụy Sĩ sản xuất) là một loại kháng thể đơn dòng có chức năng ức chế thụ thể interleukin 6 (IL-6) gây viêm. Ngoài điều trị viêm khớp dạng thấp cho người lớn, thuốc còn được dùng để điều trị viêm khớp thiếu niên tự phát thể đa khớp (PJIA) và viêm khớp thiếu niên tự phát thể hệ thống (SJIA).
Hiện nay, hạn chế của tocilizumab là giá cả và tác dụng phụ. Tại Đức, bốn mũi tiêm có giá 1.900 euro và 12 mũi tiêm có giá 5.800 euro. Một số tác dụng phụ của thuốc có thể nghiêm trọng bao gồm nhiễm trùng đường hô hấp trên, tăng cholesterol máu, chóng mặt, nhức đầu, viêm mô tế bào, loét miệng, viêm dạ dày, ngứa da, giảm bạch cầu...
Tháng 4-2020, Công ty Roche bắt đầu thử nghiệm lâm sàng giai đoạn 3 thuốc Actemra trên bệnh nhân COVID-19 - Ảnh: healthpharma.gr
Cuộc thử nghiệm COVACTA của Roche
Sau khi các bác sĩ Trung Quốc ở tuyến đầu báo cáo thuốc Actemra (tocilizumab) đã mang lại kết quả tích cực trong quá trình kiểm soát viêm phổi nặng nơi bệnh nhân COVID-19, Ủy ban Y tế quốc gia Trung Quốc đã bổ sung Actemra vào danh mục hướng dẫn điều trị COVID-19 được cập nhật đầu tháng 3-2020.
Nhân cơ hội này, nhà sản xuất Roche ở Thụy Sĩ quyết định đi theo hướng thử nghiệm lâm sàng thay vì chỉ cung cấp Actemra như trước. Trung tuần tháng 3-2020, Roche thông báo đã phối hợp với Cục Quản lý thực phẩm và dược phẩm Mỹ (FDA) và đối tác Cơ quan Nghiên cứu và phát triển y sinh tiên tiến (BARDA thuộc Bộ Y tế Mỹ) bắt đầu thử nghiệm lâm sàng giai đoạn 3 thuốc Actemra để điều trị bệnh phổi nặng cho bệnh nhân COVID-19 đang nằm viện. Dự kiến vào đầu tháng 4 sẽ bắt đầu cho bệnh nhân đăng ký tham gia thử nghiệm tại nhiều nơi trên thế giới.
Cuộc thử nghiệm COVACTA được tiến hành theo phương pháp ngẫu nhiên, mù đôi và kiểm soát bằng giả dược. Hai nhóm dùng Actemra và giả dược gồm tổng cộng 330 bệnh nhân. Các nhà nghiên cứu sẽ theo dõi bệnh nhân trong 60 ngày, sau đó phân tích bước đầu về hiệu quả của thuốc. Công ty Roche đã nhận được yêu cầu từ các cơ quan chính phủ của nhiều nước về khả năng sẵn sàng sử dụng thuốc Actemra điều trị bệnh nhân COVID-19 bị viêm phổi nặng.
Actemra được Mỹ xét duyệt lần đầu tiên về điều trị viêm khớp dạng thấp và năm 2017 được bổ sung thêm chức năng điều trị hội chứng phóng thích cytokine (CRS), một phản ứng quá mức có thể gây tử vong của hệ miễn dịch nơi bệnh nhân đang điều trị ung thư bằng liệu pháp tế bào CAR-T (tế bào lympho-T chứa thụ thể kháng nguyên dạng khảm).
Hiện nay, các nhà khoa học Trung Quốc vẫn đang tiếp tục thử nghiệm lâm sàng Actemra trong điều trị COVID-19. Đại học Khoa học và công nghệ đang nghiên cứu so sánh Actemra với cách điều trị thông thường nơi 188 bệnh nhân. Một nhóm khác tại bệnh viện số một Đại học Bắc Kinh thử nghiệm sử dụng Actemra kết hợp với thuốc trị cúm Avigan (hoạt chất favipiravir) do Công ty Fujifilm (Nhật) sản xuất.
Tuy nhiên, các nghiên cứu đến thời điểm này vẫn chưa được cơ quan chức năng khẳng định kết quả chính thức. Người dân không được tự ý sử dụng vì có thể dẫn đến tác dụng phụ ngoài ý muốn.
Ngày 30-3, Tập đoàn dược phẩm Sanofi (Pháp) thông báo bắt đầu chương trình thử nghiệm lâm sàng thứ hai giai đoạn 2/3 về thuốc trị viêm khớp dạng thấp Kevzara (sarilumab) cho bệnh nhân nhiễm COVID-19 nặng ngoài nước Mỹ. Mục đích nhằm đánh giá tính an toàn và hiệu quả của một liều Kevzara tiêm tĩnh mạch kết hợp với chăm sóc hỗ trợ thông thường (hỗ trợ hô hấp) so với dùng giả dược kết hợp với chăm sóc hỗ trợ thông thường. Chương trình thử nghiệm thứ nhất được tiến hành ở Mỹ vào đầu tháng 3-2020.
Đây là chương trình thử nghiệm toàn cầu do Sanofi kết hợp với Công ty công nghệ sinh học Regeneron (Mỹ) triển khai tại Ý, Tây Ban Nha, Đức, Pháp, Canada, Nga và Mỹ - các quốc gia đang bị đại dịch COVID-19 ảnh hưởng. Regeneron phụ trách thử nghiệm ở Mỹ còn Sanofi lo ở các nước còn lại.
Thuốc ức chế miễn dịch Kevzara (sarilumab) do Sanofi hợp tác với Regeneron phát triển. Thuốc được bán ra thị trường năm 2017 để điều trị viêm khớp dạng thấp. Kevzara là kháng thể đơn dòng hoạt động bằng cách ức chế thụ thể interleukin 6 (IL-6) gây viêm như tocilizumab. IL-6 có thể giữ vai trò trong phản ứng viêm phổi của bệnh nhân nhiễm COVID-19 nghiêm trọng hoặc nguy kịch.
____________________________________________________________
Hai lão tướng từng lăn lộn nhiều năm chống bệnh AIDS đã được điều động chống đại dịch COVID-19 ở Mỹ và Pháp. Kinh nghiệm của họ có thể góp phần tìm ra văcxin và thuốc điều trị COVID-19.
Kỳ tới: Hai lão tướng chống AIDS trên mặt trận COVID-19



















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận