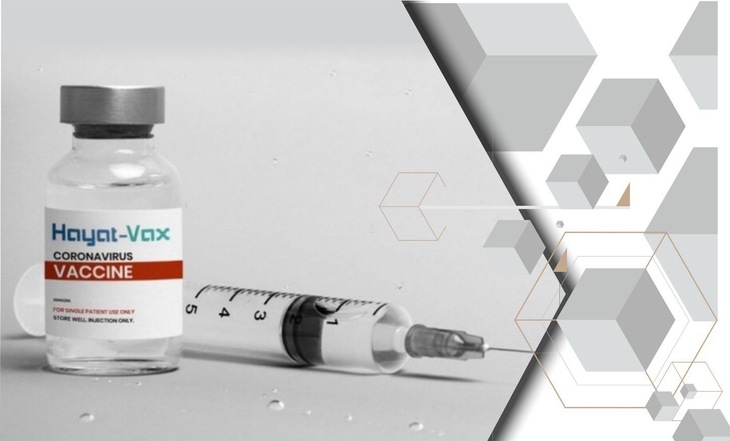
Vắc xin Hayat-Vax - Ảnh: VIMEDIMEX
Trả lời báo chí, PGS-TS Trịnh Văn Lẩu, nguyên Viện trưởng Viện Kiểm nghiệm thuốc trung ương, đã thông tin.
Ngày 10-9 vừa qua, Bộ Y tế phê duyệt có điều kiện vắc xin COVID-19 Hayat-Vax cho nhu cầu cấp bách trong phòng, chống dịch bệnh COVID-19 tại Việt Nam, theo quy định tại Điều 67, Nghị định 54 ngày 8-5-2017 của Chính phủ.
Ngày 16-9, Cục quản lý Dược đã cấp phép nhập khẩu 30 triệu liều vắc xin Hayat-Vax cho Công ty cổ phần y dược phẩm Vimedimex.
PGS-TS Trịnh Văn Lẩu, nguyên Viện trưởng Viện Kiểm nghiệm thuốc trung ương, nguyên Chủ tịch Hội đồng Dược điển Việt Nam, nói:
Vắc xin COVID-19 bất hoạt (Vero Cell) được tạo ra từ chủng SARS-CoV-2, 19nCoV-CDC-Tan-HB02, được cấy vào tế bào Vero để nuôi cấy, thu hoạch, bất hoạt bằng β-propiolactone, sau khi cô đặc và tinh chế, được hấp phụ tá dược nhôm hydroxyd để tạo thành vắc xin dạng lỏng.
Vắc xin không chứa kháng sinh và chất bảo quản, thành phần hoạt tính: SARS-CoV-2, chủng 19nCoV-CDC-Tan-HB02 (bất hoạt); Chất bổ trợ: Chất bổ trợ nhôm hydroxit; Tá dược: Dinatri hydrophosphate, Natri clorid, Natri dihydrogen photphat.
Mỗi bơm tiêm đóng sẵn/ lọ chứa 0,5mL sản phẩm cho mỗi lần dùng, mỗi liều chứa 6,5U kháng nguyên SARS-CoV-2 bất hoạt và 0,3-0,6 mg/ml tá dược nhôm hydroxyd.

PGS-TS Trịnh Văn Lẩu, nguyên viện trưởng Viện Kiểm nghiệm thuốc trung ương - Ảnh: NVCC
Ông đánh giá như thế nào về chất lượng, độ an toàn, hiệu quả của vắc xin Hayat-Vax?
Vắc xin bất hoạt được phát hiện và nghiên cứu đầu tiên trên thế giới, do một bác sĩ người Anh tên Edward Jenner tìm ra từ 1796, sau đó được nhà khoa học Louis Pasteur tiếp tục ứng dụng và phát triển.
Đến nay công nghệ sản xuất vắc xin bất hoạt đã đạt được nhiều thành tựu, góp phần bảo vệ con người trước dịch bệnh và đạt độ an toàn khi sử dụng. Loại vắc xin này được sản xuất bằng việc nuôi cấy tác nhân, sau đó dùng nhiệt hoặc hóa chất để bất hoạt chúng.
Tác nhân gây bệnh không còn sống nên không có khả năng phát triển, nhân lên và gây bệnh. Các nhà cung cấp vắc xin sẽ nghiên cứu để tiêm lượng vắc xin cần thiết với lượng kháng nguyên tương ứng đủ để tạo khả năng miễn dịch. Các loại vắc xin bất hoạt hiện vẫn đang sử dụng hiệu quả như vắc xin ho gà, thương hàn, tả, dịch hạch, bại liệt, bệnh dại, cúm, viêm gan A.
Sự ra đời của vắc xin bất hoạt ngừa dịch hạch, tả, thương hàn đã góp phần chống lại 3 đại dịch lớn trên thế giới. Vắc xin Hayat-Vax là vắc xin bất hoạt, mang ưu điểm của loại công nghệ này: Khả năng bảo vệ chống lại bệnh tật cao nếu tuân thủ liều lượng và có liều nhắc lại. Có thể được đông khô để thuận tiện cho việc vận chuyển. Có thể dùng cho những người có vấn đề về miễn dịch. An toàn và ổn định hơn so với vắc xin sống giảm độc lực.
Tính an toàn của vắc xin Hayat-Vax được đánh giá thông qua các thử nghiệm lâm sàng tại Trung Quốc và quốc tế. Thử nghiệm lâm sàng giai đoạn tại Trung Quốc được kiểm soát song song ngẫu nhiên, mù đôi và giả dược để đánh giá sơ bộ tính an toàn, khả năng sinh miễn dịch của sản phẩm, cho người lớn từ 18 tuổi trở lên.
Thử nghiệm lâm sàng giai đoạn quốc tế, cụ thể là UAE thực hiện thử nghiệm lâm sàng 4Humanity. Đây là một thử nghiệm quốc tế đa trung tâm, đa chủng tộc, thu hút các tình nguyện viên đến từ hơn 125 quốc gia (trong tổng số hơn 45.000 tình nguyện viên), tình nguyện viên được ngẫu nhiên, mù đôi, được kiểm soát song song với giả dược để đánh giá hiệu quả bảo vệ, tính an toàn và khả năng sinh miễn dịch của sản phẩm này.
Theo dõi dữ liệu an toàn từ 0 - 21/28 ngày sau mỗi lần tiêm để quan sát sự xuất hiện của các tác dụng phụ, chú ý đến các tác dụng phụ nghiêm trọng xảy ra trong vòng 12 tháng sau khi tiêm chủng đủ liệu trình cùng một lúc. Dữ liệu phân tích tạm thời cho thấy, chế độ tiêm chủng hai liều cách nhau 21 (+7) ngày, hiệu quả của vắc xin chống lại COVID-19 là 78,89% (KTC 95%: 65,79% - 86,97%).
Mức độ nghiêm trọng của tác dụng không mong muốn đối với sản phẩm này được quan sát trong các thử nghiệm lâm sàng chủ yếu là cấp độ 1 (mức nhẹ), tỉ lệ mắc tác dụng không mong muốn cấp độ 3 trở lên là 0,54%, không có tác dụng không mong muốn cấp độ 4 liên quan Hayat-Vax được báo cáo.
Tác dụng không mong muốn cấp độ 3 tại chỗ tiêm được báo cáo trong các thử nghiệm lâm sàng như đau, phát ban, ngứa; Tác dụng không mong muốn toàn thân cấp độ 3 sau tiêm chủng là sốt, mệt mỏi, nhức đầu, đau cơ, đau khớp, ho, khó thở, buồn nôn, nôn, tiêu chảy, táo bón, khó nuốt.
Một số vắc xin tương tự Hayat có hạn sử dụng là 24 tháng, trong khi đó Hayat-Vax có hạn sử dụng 12 tháng, vậy sự khác biệt ở hai loại vắc xin này được sản xuất cùng một công nghệ là như thế nào?
Như trên tôi đã nói, vắc xin Hayat-Vax công bố hạn sử dụng dựa trên dữ liệu thật về nghiên cứu độ ổn định của sản phẩm là 12 tháng.
Ông có thể cho biết vắc xin Hayat-Vax được thử nghiệm miễn dịch kháng nguyên bằng phương pháp nào?
Vắc xin Hayat-Vax được sử dụng phương pháp thử nghiệm kháng nguyên ELISA gián tiếp, đây là phương pháp thử nghiệm miễn dịch theo liên kết enzym, phương pháp này đã được Tổ chức Y tế thế giới (WHO) phê duyệt sử dụng để xác định kháng nguyên COVID-19.

Vắc xin Hayat-Vax - Ảnh: VIMEDIMEX
ELISA gián tiếp cho độ nhạy cao, chỉ cần tạo một loại kháng kháng thể mang enzyme để nhận biết cho nhiều kháng nguyên khác nhau. ELISA gián tiếp khác ELISA trực tiếp ở chỗ kháng thể bắt kháng nguyên không được gắn enzyme, mà nó là mục tiêu gắn đặc hiệu của một kháng thể khác (kháng thể này mới là kháng thể được gắn với enzyme). Vấn đề này đã được mô tả trong hồ sơ của đề cương tóm tắt và thử nghiệm cho từng lô vắc xin Hayat-Vax, được phê duyệt mô tả thử nghiệm "in-vitro" - thử nghiệm trong phòng thí nghiệm - đo nồng độ của kháng nguyên trong hồ sơ và lô xuất xưởng.
Đặc biệt hơn, vắc xin Hayat-Vax được thực hiện quy trình kiểm tra chất lượng, an toàn và hiệu quả rất nghiêm nghặt, cụ thể:
Lần đầu tiên, do Sinopharm (nhà sản xuất bán thành phẩm Hayat-Vax) thực hiện kiểm tra chất lượng bán thành phẩm, theo tiêu chuẩn kỹ thuật đã được Sinopharm hoặc WHO phê duyệt trước khi vận chuyển đến UAE.
Lần thứ 2, Bộ Y tế UAE tiếp nhận kiểm tra và xác nhận "đạt tiêu chuẩn kỹ thuật".
Lần thứ 3, Gulf Pharmaceutical Industries (nhà sản xuất dược phẩm thực hiện công đoạn sản xuất thành phẩm Hayat-Vax) tại UAE thực hiện thêm một lần kiểm tra chất lượng, trước khi phân liều và đóng gói vào lọ.
Lần thứ 4, Bộ Y tế UAE kiểm tra chất lượng và phê duyệt từng lô vắc xin Hayat-Vax để xuất khẩu, trước khi chuyển hàng sang Việt Nam
Lần thứ 5, trước khi nhập khẩu, những lô vắc xin Hayat-Vax đầu tiên về Việt Nam dự kiến vào cuối tuần tới. Cơ sở sản xuất Julphar (Gulf Pharmaceutical Industries tại UAE) đã gửi đề cương tóm tắt và thử nghiệm của lô vắc xin Hayat-Vax cho đơn vị nhập khẩu (Công ty Vimedimex).
Đơn vị nhập khẩu đã phối hợp với các chuyên gia của Viện Kiểm định quốc gia vắc xin và sinh phẩm y tế thực hiện thẩm định trước hồ sơ chất lượng những lô vắc xin, kết quả trên hồ sơ cho thấy những lô vắc xin này, hoạt lực tương đối InVitro từ 0.5-2.0 của từng lô vắc xin Hayat-Vax đều chứa trong khoảng 6.5U kháng nguyên SARS-CoV-2 (tế bào vero) bất hoạt.
Lần thứ 6, sau khi vắc xin Hayat-Vax nhập khẩu về Việt Nam, Viện Kiểm định quốc gia vắc xin và sinh phẩm y tế sẽ thực hiện lấy mẫu vắc xin Hayat–Vax, tiến hành kiểm định và cấp giấy chứng nhận xuất xưởng lô vắc xin Hayat-Vax trước khi đưa vào sử dụng.

















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận