
Thứ trưởng Bộ NN&PTNT trao giấy chứng nhận lưu hành vắc xin dịch tả heo châu Phi - Ảnh: CHÍ TUỆ
Chiều 3-6, Bộ Nông nghiệp và phát triển nông thôn (NN&PTNT) tổ chức lễ công bố kết quả nghiên cứu, sản xuất thành công vắc xin phòng bệnh DTHCP (vắc xin thương mại NAVET-ASFVAC do Công ty cổ phần Thuốc thú y trung ương Navetco sản xuất).
Phát biểu tại buổi lễ, Thứ trưởng Bộ NN&PTNT Phùng Đức Tiến cho biết đầu tháng 11-2019, ngay sau khi các nhà khoa học của Hoa Kỳ công bố nghiên cứu thành công chủng virus DTHCP nhược độc đã được cắt bỏ đoạn gene ASF-G-Delta I177L, lãnh đạo Bộ NN&PTNT đã cử lãnh đạo Cục Thú y sang Hoa Kỳ dự họp, gặp trực tiếp với các chuyên gia Hoa Kỳ để bàn phối hợp nghiên cứu, sản xuất vắc xin DTHCP.
Đến nay, tại Việt Nam đã có 3 doanh nghiệp tiên phong, có đủ tiềm lực, đầu tư nghiêm túc để nghiên cứu, sản xuất thành công vắc xin DTHCP bao gồm Công ty cổ phần Thuốc thú y trung ương Navetco (Công ty Navetco), Công ty TNHH MTV AVAC, Công ty cổ phần tập đoàn Dabaco.
Ngay sau khi tiếp nhận chủng giống ASF-G-Delta I177L từ Bộ Nông nghiệp Hoa Kỳ vào tháng 9-2020, Công ty Navetco đã khẩn trương triển khai nghiên cứu, trải qua 5 lần thử nghiệm trong phòng thí nghiệm.
Kết quả 100% số heo tiêm vắc xin được bảo hộ khi công cường độc trong phòng thí nghiệm. Trong điều kiện sản xuất đã bảo hộ được trên 80% số heo được tiêm vắc xin khi công cường độc với chủng virus gây bệnh DTHCP tại Việt Nam, độ dài miễn dịch của vắc xin kéo dài 6 tháng sau tiêm phòng.
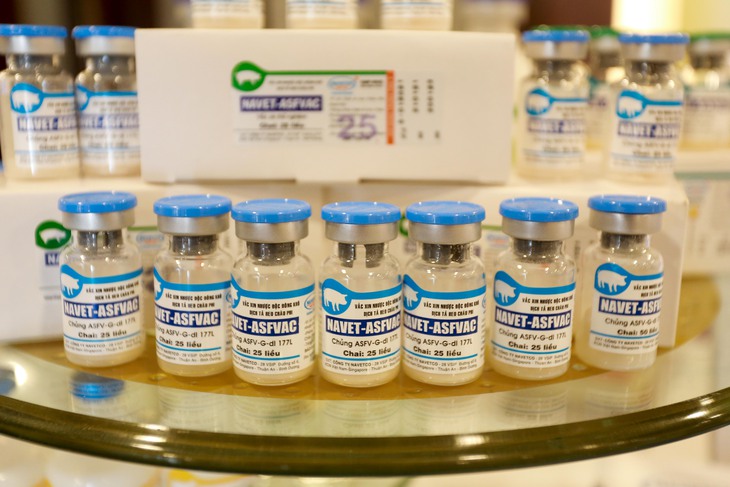
Vắc xin phòng dịch tả heo châu Phi do Công ty Navetco sản xuất - Ảnh: CHÍ TUỆ
Đối với vắc xin DTHCP AVAC ASF LIVE (Công TNHH MTV AVAC nghiên cứu) đạt tiêu chuẩn về vô trùng, an toàn và hiệu lực bảo hộ đạt trên 80% số heo thí nghiệm, độ dài miễn dịch của vắc xin kéo dài 4 tháng sau tiêm phòng đối với heo thịt từ 4 tuần tuổi trở lên.
Từ tháng 3-2022 đến nay, Bộ NN&PTNT đã chỉ đạo tổ chức đánh giá sử dụng vắc xin DTHCP AVAC ASF LIVE trong điều kiện sản xuất, tại các trang trại chăn nuôi heo có quy mô khác nhau.
Đối với Công ty Dabaco đã nghiên cứu, sản xuất được vắc xin DTHCP nhược độc đông khô, đã thử nghiệm vắc xin trên đàn heo của tập đoàn. Kết quả cho thấy vắc xin đạt tiêu chuẩn về an toàn và hiệu lực bảo hộ trên 80% trên đàn heo thí nghiệm. Đã sản xuất thành công vắc xin thương mại dạng đông khô DACOVAC-ASF2 và hiện nay đang được kiểm nghiệm, đánh giá chất lượng, đăng ký lưu hành theo quy định.
Bộ trưởng Bộ NN&PTNT Lê Minh Hoan đề nghị các doanh nghiệp sản xuất vắc xin cân bằng lợi nhuận, đưa ra mức giá bán hợp lý để người chăn nuôi có thể tiếp cận dễ dàng.
Trao đổi với báo chí bên lề lễ công bố, ông Trần Xuân Hạnh, phó tổng giám đốc Công ty Navetco, cho biết trong giai đoạn 1, vắc xin do công ty sản xuất sẽ sử dụng ở diện hẹp với số lượng vắc xin dự kiến được phép sử dụng 600.000 liều.
Trong giai đoạn 2, sau khi có báo cáo đánh giá kết quả sử dụng vắc xin ở giai đoạn 1, Cục Thú y sẽ tham mưu Bộ Nông nghiệp và phát triển nông thôn chỉ đạo sử dụng vắc xin ở phạm vi toàn quốc.
Dự kiến sẽ lưu hành trên thị trường vào cuối tháng 8 và giá vắc xin DTHCP sẽ từ 34.000 - 36.000 đồng/liều.




















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận