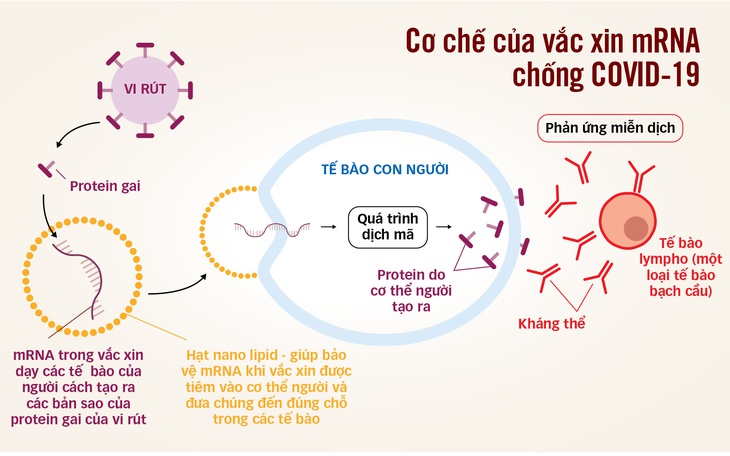
Nguồn: The Conversation, Cục Y tế dự phòng - Tổng hợp: Minh Khôi - Đồ họa: TẤN ĐẠT
Việc vắc xin mRNA giành giải Nobel không gây bất ngờ với giới chuyên môn vì đó là phần thưởng xứng đáng.
Phát hiện đột phá
Trong tuyên bố ngày 2-10, Hội đồng Nobel tại Viện Karolinska (Thụy Điển) cho biết những phát hiện đột phá của hai nhà khoa học Katalin Karikó và Drew Weissman đã thay đổi căn bản sự hiểu biết về cách mRNA tương tác với hệ thống miễn dịch.
Khi bà Karikó và ông Weissman công bố nghiên cứu về công nghệ mRNA vào năm 2005, nó hầu như không được quan tâm mấy. Tuy nhiên, khi xảy ra đại dịch COVID-19 vào năm 2020, công nghệ này đã đặt nền tảng quan trọng trong cuộc chiến chống dịch: vắc xin.
Ông Rickard Sandberg, thành viên của ban trao giải, cho biết vắc xin mRNA cùng với các loại vắc xin COVID-19 khác đã được tiêm hơn 13 tỉ lần, giúp cứu sống hàng triệu người, ngăn chặn bệnh nặng, giảm gánh nặng bệnh tật nói chung và giúp thế giới mở cửa trở lại.
Để hiểu được tính đột phá của giải Nobel y sinh năm nay cần quay trở lại những vắc xin mà con người đã sử dụng từ trước đó.
Con người đã sử dụng vắc xin dựa trên vi rút đã chết hoặc bị suy yếu để chống lại những căn bệnh như bại liệt, sởi và sốt vàng da. Sau đó nhờ những tiến bộ trong sinh học phân tử trong những thập niên gần đây, vắc xin vector dùng mã di truyền vi rút để chống lại vi rút viêm gan B hay Ebola.
Tuy nhiên, các công nghệ này đòi hỏi phải nuôi cấy tế bào quy mô lớn, sử dụng nhiều tài nguyên dẫn đến khó sản xuất vắc xin nhanh chóng để đối phó với các đợt bùng dịch như COVID-19.
Trong tế bào của chúng ta, thông tin di truyền mã hóa trong ADN được chuyển sang messenger RNA (mRNA) để làm "khuôn" sản xuất protein.
Trong những năm 1980, các phương pháp hiệu quả để sản xuất mRNA mà không cần nuôi cấy tế bào đã ra đời, giúp đẩy nhanh sự phát triển các ứng dụng sinh học phân tử trong một số lĩnh vực.
Tuy nhiên, ý tưởng sử dụng công nghệ mRNA cho mục đích điều trị và chế tạo vắc xin vẫn còn nhiều rào cản phía trước. mRNA được tổng hợp trong ống nghiệm không ổn định và khó phân phối, hơn nữa nó có thể gây ra phản ứng viêm.
Dù vậy, những khó khăn này không làm nhà khoa học người Hungary Karikó nản lòng. Vào đầu những năm 1990, khi còn là trợ lý giáo sư tại Đại học Pennsylvania (Mỹ), bà vẫn giữ vững quyết tâm hiện thực hóa mRNA như một phương pháp trị liệu mặc dù gặp khó khăn trong việc thuyết phục các nhà tài trợ nghiên cứu.
Bà Karikó sau đó nhận được sự ủng hộ từ một đồng nghiệp mới tại trường đại học là nhà miễn dịch học Drew Weissman (người Mỹ). Ông là người quan tâm đến các tế bào đuôi gai, có chức năng quan trọng trong việc giám sát miễn dịch và kích hoạt các phản ứng miễn dịch từ vắc xin.
Từ đó, sự hợp tác của họ tập trung vào cách các loại RNA khác nhau tương tác với hệ thống miễn dịch.

Hai nhà khoa học Katalin Karikó (phải) và Drew Weissman tại Đại học Pennsylvania - Ảnh: Reuters
Mở ra cơ hội chữa ung thư, lupus
Hai nhà khoa học Karikó và Weissman nhận thấy rằng các tế bào đuôi gai coi mRNA được sản xuất trong ống nghiệm là một chất lạ, dẫn đến việc chúng kích hoạt và giải phóng các phân tử tín hiệu viêm.
Trong khi đó, mRNA từ tế bào động vật có vú lại không gây ra phản ứng tương tự. Karikó và Weissman nhận ra rằng một số đặc tính quan trọng giúp phân biệt các loại mRNA khác nhau.
Hai người nhận thấy các base trong RNA (RNA chứa bốn base, viết tắt là A, U, G và C) từ tế bào động vật có vú thường xuyên bị biến đổi về mặt hóa học, trong khi mRNA tạo ra từ ống nghiệm thì không.

GS Katalin Karikó trong buổi trò chuyện với sinh viên tại Trường đại học VinUni ngày 21-1-2022 - Ảnh: Quỹ VinFuture
Để nghiên cứu liên quan giữa các base và phản ứng viêm, họ đã tạo ra các biến thể khác nhau của mRNA, mỗi biến thể có những thay đổi hóa học riêng biệt trong các base. Kết quả thật đáng ngạc nhiên: phản ứng viêm gần như bị loại bỏ khi các base được chỉnh sửa được đưa vào mRNA.
Karikó và Weissman hiểu rằng khám phá của họ có ý nghĩa sâu sắc đối với việc sử dụng mRNA để chữa bệnh. Họ đã công bố những kết quả quan trọng này vào năm 2005, 15 năm trước khi đại dịch COVID-19 xảy ra.
Trong các nghiên cứu sâu hơn được công bố vào năm 2008 và 2010, cả hai đã chỉ ra mRNA chỉnh sửa còn làm tăng đáng kể việc sản xuất protein so với mRNA không được sửa đổi. Với kết quả này, Karikó và Weissman đã loại bỏ những trở ngại quan trọng trên con đường ứng dụng lâm sàng của mRNA.
Messenger RNA (mRNA) là một chuỗi mã di truyền mà tế bào có thể "đọc" và sử dụng để tạo ra protein. Khi được dùng làm vắc xin, mRNA hướng dẫn các tế bào trong cơ thể tạo ra mảnh protein gai giống của vi rút.
Điều này sẽ "dạy" cho hệ thống miễn dịch phát hiện và nhận ra nó là vật lạ và sẵn sàng tấn công khi vi rút thật xâm nhập vào cơ thể. Công nghệ này được chọn vì nó có thể phát triển nhanh chóng. Các nhà sản xuất thậm chí không cần vi rút thật mà chỉ cần trình tự gene để tạo ra vắc xin.
"Thật ra đã có những thử nghiệm lâm sàng trước COVID-19, nhưng mọi người không biết", bà Karikó tiết lộ sau khi biết mình đoạt giải Nobel. Theo đó, vắc xin mRNA đã được thử nghiệm cho các bệnh khác như sốt rét, cúm và bệnh dại, nhưng đại dịch đã thu hút nhiều sự chú ý hơn đến phương pháp này.

GS Drew Weissman trong buổi giao lưu tại Trường đại học VinUni ngày 21-1-2022 - Ảnh: Quỹ VinFuture
Trong đại dịch COVID-19, hai loại vắc xin mRNA (Pfizer và Moderna) được báo cáo có tỉ lệ bảo vệ lên đến 95% và được phê duyệt sớm từ cuối năm 2020.
Tính linh hoạt và tốc độ phát triển ấn tượng của vắc xin mRNA được kỳ vọng sẽ mở đường cho việc tạo ra vắc xin chống lại các bệnh truyền nhiễm khác, protein trị liệu hoặc điều trị một số bệnh ung thư.
Giáo sư Paul Hunter, Đại học East Anglia (Anh), cho rằng vắc xin mRNA là yếu tố quyết định giúp chấm dứt đại dịch. "Nếu không có công nghệ mRNA, dịch COVID-19 có thể còn tệ hơn nhiều", Hãng tin AP dẫn lời ông Hunter nói.
Còn giáo sư Bharat Pankhania (Đại học Exeter) cho rằng ưu điểm lớn của vắc xin mRNA là có thể sản xuất với số lượng lớn.
Ông Pankhania dự đoán công nghệ này có thể được sử dụng để cải tiến vắc xin cho các bệnh khác như Ebola, sốt rét và sốt xuất huyết, đồng thời cũng có thể giúp con người tạo miễn dịch chống lại một số loại ung thư hoặc các bệnh tự miễn dịch như bệnh lupus.
"Chúng ta có thể tiêm vắc xin chống lại các protein ung thư bất thường cho mọi người... Đó là một công nghệ có mục tiêu rõ ràng hơn nhiều so với trước đây và có thể cách mạng hóa cách chúng ta xử lý không chỉ các đợt bùng phát mà cả các bệnh không lây nhiễm", ông Pankhania đánh giá.
Bà Katalin Karikó, sinh năm 1955, ở Hungary, là trợ lý giáo sư Đại học Pennsylvania đến năm 2013. Sau đó, bà trở thành phó chủ tịch cấp cao tại Công ty công nghệ sinh học BioNTech của Đức. Từ năm 2021, bà là giáo sư tại Đại học Szeged ở Hungary và là giáo sư kiêm nhiệm tại Trường Y Perelman thuộc Đại học Pennsylvania (Mỹ).
Ông Drew Weissman, sinh năm 1959, ở Massachusetts, Mỹ. Ông được đào tạo tại Đại học Boston, Harvard và nghiên cứu sau tiến sĩ tại Viện Y tế quốc gia. Năm 1997, ông thành lập nhóm nghiên cứu của mình tại Trường y Perelman thuộc Đại học Pennsylvania. Ông là giám đốc Viện đổi mới RNA của Đại học Pennsylvania.
Chủ nhân Giải thưởng VinFuture năm 2021

Thủ tướng Phạm Minh Chính trao giải thưởng VinFuture 3 triệu USD cho ba nhà khoa học: Katalin Karikó (bìa phải), Drew Weissman (thứ hai từ trái sang) và Pietter Rutter Cullis với công nghệ nghiên cứu vắc xin mRNA tối 20-1-2022 - Ảnh: NAM TRẦN
Trước khi đoạt Giải Nobel 2023, nghiên cứu của GS Katalin Karikó và Drew Weissman đã được Quỹ VinFuture tôn vinh với Giải thưởng VinFuture năm 2021, cùng GS Pieter Rutter Cullis.
Mặc dù đã được vinh danh bởi nhiều giải thưởng quốc tế lớn, Giải thưởng VinFuture vẫn có vị trí đặc biệt đối với GS Karikó. Trong một chia sẻ vào cuối tháng 6-2023, bà nhấn mạnh tầm quan trọng của việc có những giải thưởng khoa học đến từ các quốc gia đang phát triển, đặc biệt là những giải thưởng có uy tín, vì sẽ thu hút sự chú ý không chỉ ở trong nước mà còn trên phạm vi toàn cầu.
Bà Karikó khẳng định rằng từ VinFuture, các nhà khoa học thế giới đã hiểu hơn về một Việt Nam đang mạnh mẽ vươn ra quốc tế. Những giải thưởng quốc tế như VinFuture không chỉ là nguồn cảm hứng cho những nhà khoa học nội địa mà còn tạo nên sức hút, sự quan tâm từ các quốc gia có nền khoa học và công nghệ phát triển mạnh, từ đó mở ra cơ hội cho sự hợp tác và chia sẻ kiến thức, đẩy mạnh tiến trình phát triển khoa học công nghệ trên toàn cầu, đặc biệt ở các quốc gia đang phát triển.
Từ tháng 10-2022, GS Karikó không còn giữ chức vụ phó chủ tịch cấp cao tại BioNTech, nhưng vẫn đảm nhiệm vai trò tư vấn. Hiện tại bà đang tập trung vào một hướng nghiên cứu mới, không hoàn toàn là mRNA, nhưng vẫn có liên quan phần nào tới lĩnh vực này.
Bên cạnh đó, bà tham gia hàng loạt chuyến công tác tại nhiều viện, trường trên thế giới để thuyết giảng và chia sẻ về hành trình khoa học của mình, truyền cảm hứng cho những người trẻ đang theo đuổi lĩnh vực này.
Còn GS Drew Weissman, tại lễ trao Giải thưởng VinFuture năm 2021, chia sẻ bản thân không phải người nhận giải thưởng này mà "hàng nghìn nhà khoa học đi trước và đi sau tôi sẽ tiếp bước những nghiên cứu này, tạo ra nhiều phương pháp chữa bệnh mới, cho những căn bệnh mới".
"Đây không phải là dấu chấm của tất cả mọi thứ, mà mở ra một liệu pháp vắc xin COVID-19 mới, những thế hệ vắc xin mới cho những bệnh tật khác nhau. Và điều quan trọng nữa là sự khởi đầu của sự hợp tác giữa các quốc gia ở Đông Nam Á, trong đó có Việt Nam, Thái Lan và nhiều quốc gia khác", GS Drew Weissman nói.
Trong buổi trao đổi với Quỹ VinFuture vào tháng 12-2022, ông cho biết mình dành toàn bộ tiền thưởng nhận được cho khoa học. "Số tiền này được sử dụng để phát triển các phương pháp chữa bệnh thiếu máu hồng cầu lưỡi liềm cũng như các loại vắc xin khác mà chúng tôi đang nghiên cứu. Tôi hy vọng điều này giúp ích lớn cho khoa học cũng như cuộc sống của mọi người", ông nói.



















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận