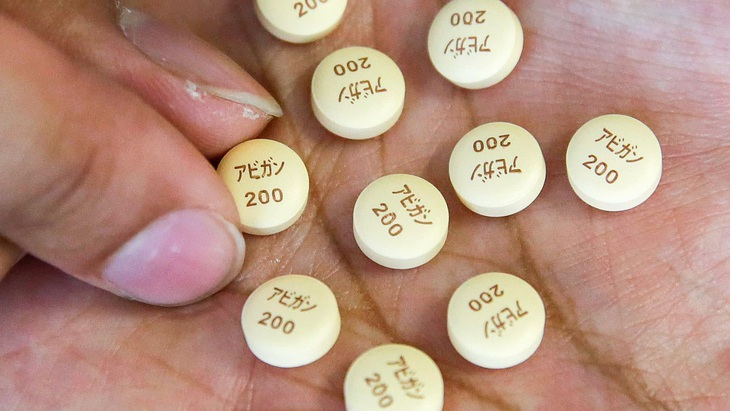
Thuốc Avigan do Công ty dược phẩm Toyama Chemical của Nhật phát triển - Ảnh: JIJI
Trong số các loại thuốc không còn giữ mục tiêu điều trị ban đầu mà chuyển hướng sang điều trị bệnh nhân COVID-19, ngoài thuốc trị sốt rét hydroxychloroquine, thuốc điều trị viêm khớp dạng thấp tocilizumab và Kevzara (sarilumab), thuốc kháng virus remdesivir điều trị Ebola, còn có thuốc chống cúm Avigan và thuốc điều trị nhiễm HIV/AIDS Kaletra.
Từ chống cúm thành thuốc điều trị COVID-19
Cuối tháng 2-2020, không khí tại trụ sở Tập đoàn Fujifilm ở Tokyo (Nhật) hết sức khẩn trương.
Ban giám đốc cùng hàng trăm nhân viên đang thực hiện một nhiệm vụ chưa từng có trong lịch sử 86 năm thành lập. Bộ trưởng Y tế Katsunobu Kato dự liệu làn sóng bệnh nhân mắc COVID-19 chắc chắn sẽ ập đến nên mời gọi Fujifilm góp sức chiến đấu. Vũ khí của Fujifilm là thuốc chống cúm Avigan. Chính phủ đã phê duyệt đưa Avigan vào điều trị COVID-19 như trường hợp điều trị khẩn cấp.
Ngày 28-3, Thủ tướng Shinzo Abe long trọng thông báo Nhật bắt đầu quy trình chính thức sử dụng thuốc Avigan như hướng dẫn điều trị chuẩn trong điều trị COVID-19. Song song đó, từ đầu tháng 4-2020 Fujifilm bắt đầu thử nghiệm lâm sàng giai đoạn 3 tại Tokyo để đánh giá tính an toàn và hiệu quả của Avigan. Thử nghiệm kéo dài đến cuối tháng 6. Có 100 bệnh nhân từ 20-74 tuổi (trừ phụ nữ mang thai) viêm phổi nhẹ dùng Avigan trong 14 ngày.
Avigan có chứa hoạt chất kháng virus favipiravir. Các thuốc điều trị cúm khác ức chế virus lây lan bằng cách ngăn chặn kháng nguyên neuraminidase của virus. Ngược lại, favipiravir là hoạt chất duy nhất ức chế trực tiếp phân tử polymerase trong bộ gen ARN của virus để ngăn chặn virus sao chép, từ đó virus không thể lây lan được nữa.
Năm 1990, khi bắt đầu hợp tác với GS virus học Kimiyasu Shiraki, Công ty dược phẩm Toyama Chemical (chi nhánh của Tập đoàn Fujifilm) dự kiến nghiên cứu một hợp chất kháng virus mới điều trị mụn rộp. Tám năm sau, GS Shiraki phát hiện hợp chất có tiềm năng trị bệnh cúm. Từ đó thuốc favipiravir ra đời.
Năm 2014, Cơ quan Thiết bị y tế và dược phẩm Nhật cấp phép lưu hành thuốc favipiravir. Cuối năm đó, vào thời điểm dịch Ebola giết chết hàng ngàn người ở Tây Phi, favipiravir đã được sử dụng tại khu vực này trong khuôn khổ "nghĩa vụ từ bi". Tại Guinea, khi cho bệnh nhân nhiễm Ebola có lượng virus từ thấp đến trung bình dùng favipiravir, tỉ lệ tử vong đã giảm từ 30% còn 15% (50%).
Hiện nay dù chưa có đầy đủ dữ liệu chứng minh hiệu quả của Avigan trong điều trị COVID-19, vẫn có nhiều yếu tố để lạc quan. Hôm 17-3, ông Trương Tân Dân - quan chức của Bộ Khoa học và công nghệ Trung Quốc - thông báo thuốc favipiravir "rất an toàn và hiệu quả rõ ràng" trong điều trị bệnh nhân COVID-19.
Ông công bố kết luận sơ bộ của các bác sĩ (chưa công bố dữ liệu và phương pháp luận) cho thấy tại Thâm Quyến, các bệnh nhân COVID-19 dùng favipiravir đã có kết quả âm tính sau bốn ngày thay vì 11 ngày ở nhóm đối chứng. Còn tại Vũ Hán, bệnh nhân dùng favipiravir khỏi sốt sớm gần hai ngày so với nhóm đối chứng.
Thử nghiệm lâm sàng Avigan của Tập đoàn Fujifilm ở Nhật không liên quan đến thử nghiệm lâm sàng ở Trung Quốc vì Trung Quốc dựa vào thuốc do Công ty Zhejiang Hisun Pharmaceutical sản xuất.
Công ty này trước là đối tác sản xuất của Fujifilm, nay sản xuất favipiravir ở Trung Quốc sau khi bản quyền favipiravir của Fujifilm ở Trung Quốc hết hạn hồi năm ngoái. Cuối tháng 3, Trung Quốc đã bắt đầu xuất khẩu favipiravir.
Hiện nay, nhiều nước đang lùng sục mua thuốc Avigan của Nhật. Indonesia đã cho nhập 5.000 liều Avigan và đặt mua thêm 2 triệu liều nữa. Đức sẵn sàng bỏ ra nhiều triệu USD tìm mua Avigan. Fujifilm đã thảo luận với Mỹ về khả năng thử nghiệm lâm sàng Avigan tại Mỹ.

Trong phòng thí nghiệm của Công ty AbbVie - Ảnh: Getty images
Góp sức chống đại dịch
Trong khó khăn mới biết ai có tấm lòng. Để góp sức ngăn chặn COVID-19 trên thế giới, Nhật đã sẵn sàng cho không thuốc Avigan.
Hãng tin Kyodo (Nhật) đưa tin ngày 3-4, Chánh văn phòng nội các Nhật Yoshihide Suga khẳng định: "Chúng tôi đang phối hợp để cung cấp miễn phí Avigan với số lượng cần thiết cho các quốc gia mong muốn".
Ông cho biết khoảng 30 nước đã gửi công hàm qua đường ngoại giao cho Nhật đề nghị mua Avigan để điều trị bệnh nhân COVID-19.
Tại Mỹ, Công ty nghiên cứu dược phẩm AbbVie ở North Chicago (bang Illinois) cũng bày tỏ như vậy. Báo Financial Times (Anh) ngày 23-3 đưa tin AbbVie đã tuyên bố từ bỏ bản quyền sáng chế đối với thuốc Kaletra trên toàn thế giới với hi vọng thuốc được phổ biến rộng rãi cho bệnh nhân COVID-19.
Đây là đại gia dược phẩm đầu tiên trên thế giới từ bỏ quyền sở hữu trí tuệ đối với thuốc có tiềm năng điều trị COVID-19, đồng nghĩa với bỏ đi nhiều triệu USD tiền bán thuốc.
Thuốc kháng virus Kaletra vốn được sử dụng để điều trị nhiễm HIV, kết hợp hoạt chất lopinavir (chất ức chế protease) có chức năng kháng virus và hoạt chất ritonavir có chức năng kháng retrovirus. AbbVie lưu hành Kaletra từ năm 2001. Tại một số thị trường, Kaletra mang tên biệt dược Aluvia.
Tuy nhiên, trong các loại thuốc đang thử nghiệm điều trị COVID-19 có lẽ lopinavir/ritonavir là thuốc đầu tiên vấp phải thất bại. Tạp chí New England Journal of Medicine (Mỹ) ngày 18-3 đã đăng nghiên cứu của các nhà khoa học Trung Quốc với đầu đề "Thử nghiệm lopinavir/ritonavir nơi người trưởng thành nằm viện nhiễm COVID-19 nặng".
Thử nghiệm được tiến hành tại Vũ Hán trên 199 bệnh nhân suy hô hấp và độ bão hòa oxy dưới 94% theo phương pháp mở, ngẫu nhiên, có đối chứng. Lopinavir/ritonavir (400mg/100mg) được dùng hai lần mỗi ngày trong 14 ngày kết hợp với điều trị tiêu chuẩn.
Kết quả cho thấy lopinavir/ritonavir không chứng minh hiệu quả trong điều trị các bệnh nghiêm trọng do virus SARS-CoV-2 gây ra. Ngoài ra, không có khác biệt đáng kể về tỉ lệ tử vong sau 28 ngày điều trị (19,2% ở nhóm dùng lopinavir/ritonavir và 25% ở nhóm đối chứng) cũng như tỉ lệ bệnh nhân còn ARN virus.
Tác dụng phụ về tiêu hóa xảy ra thường xuyên hơn trong nhóm dùng lopinavir/ritonavir. Ưu điểm duy nhất là các triệu chứng nghiêm trọng xuất hiện trong nhóm đối chứng thường xuyên hơn.
Dù vậy, các nhà khoa học Trung Quốc xác định sẽ tiếp tục thử nghiệm lopinavir/ritonavir. Châu Âu và WHO đã đưa lopinavir/ritonavir vào chương trình thử nghiệm lâm sàng bốn phương pháp điều trị COVID-19.
Tại Nga ngày 25-3, cơ quan y tế thành phố Matxcơva thông báo lopinavir/ritonavir đạt hiệu quả trong điều trị các ca COVID-19 nhẹ và các bác sĩ có thể kê đơn cho bệnh nhân điều trị tại nhà. Ngày 2-4, Bộ Y tế Israel cũng đã phê duyệt đưa Kaletra vào điều trị bệnh nhân COVID-19.
Không được tự ý dùng thuốc
Ngày 31-3, lần đầu tiên Cơ quan An toàn thuốc và sản phẩm y tế quốc gia Pháp (ANSM) cảnh báo đã xảy ra năm trường hợp nghiêm trọng và ba trường hợp tử vong ở Pháp do sử dụng thuốc thử nghiệm điều trị COVID-19, trong đó có thuốc trị sốt rét Plaquenil và thuốc Kaletra.
ANSM kêu gọi người dân không nên tự ý dùng thuốc hoặc dùng theo toa bác sĩ tự kê đơn ngoài bệnh viện vì Plaquenil và Kaletra gây tác dụng phụ nghiêm trọng như nguy cơ tim, nhất là dùng Plaquenil chung với kháng sinh azithromycin.
Đối với Plaquenil (hydroxychloroquine) và Nivaquine (chloroquine), ANSM lưu ý nhiều rủi ro nghiêm trọng như nhiễm độc da, hạ đường huyết nặng, rối loạn tâm thần, rối loạn nhịp tim.
Ngoài ra, thuốc sẽ tăng độc tính nếu sử dụng chung với một số thuốc điều trị thông thường khác như nhóm kháng sinh (macrolid, fluoroquinolone), citalopram (Seropram), escitalopram (Seroplex), hydroxyzine (Atarax), domperidone (Motilium).
Trong khi các nhà khoa học thế giới đang chạy đua tìm "thần dược" chữa Covid-19 thì bệnh nhân đại dịch này ở Việt Nam được chữa trị thế nào?
Kỳ tới: Điều trị bệnh nhânCovid-19 ở Việt Nam



















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận