 Phóng to Phóng to |
|
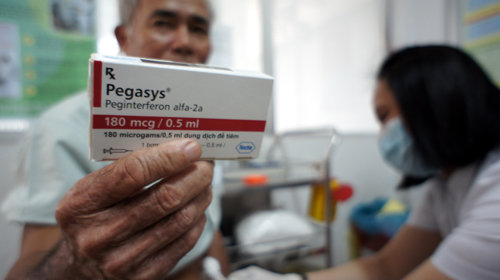
Thuốc Pegasys của Hãng Roche (Thụy Sĩ) trị viêm gan siêu vi C mãn tính có giá hơn 2,2-2,8 lần so với thuốc trong nước sản xuất - Ảnh: N.C.T. |
Nhà sản xuất thuốc Pegnano là Công ty TNHH công nghệ sinh học dược Nanogen (gọi tắt là Công ty Nanogen). Mỗi dược phẩm Pegnano có chứa 180mcg Peginterferon alfa-2a, dùng để điều trị bệnh viêm gan siêu vi B và C mãn tính ở người lớn.
Yêu cầu chấm dứt sản xuất
|
Chưa nhận được khiếu nại Theo ông Phạm Mạnh Hào - chánh văn phòng Cục Sở hữu trí tuệ, các cuộc tranh chấp về sở hữu trí tuệ nên đưa đến một cơ quan giám định là Viện Khoa học sở hữu trí tuệ xem xét. Sau khi xác định có vi phạm, bên khiếu nại có thể đưa vụ việc ra tòa án hoặc thanh tra Bộ Khoa học - công nghệ. Hiện khiếu nại của Roche cũng chưa gửi đến Cục Sở hữu trí tuệ. Theo nguồn tin của Tuổi Trẻ, Bộ Y tế sẽ thành lập một tổ công tác để đánh giá lại toàn bộ vụ việc. WHO: không cấm Theo Tổ chức Y tế thế giới (WHO), hiệp ước “Những khía cạnh trao đổi mua bán của quyền sở hữu trí tuệ” không cấm các chính phủ sản xuất các sản phẩm thay thế (generic). Việc cạnh tranh giữa các hãng dược phẩm và các nhà sản xuất generic, theo WHO, tỏ ra có hiệu quả hơn việc mặc cả giảm giá các mặt hàng dược phẩm, đặc biệt là thuốc chữa HIV/AIDS. Tại Thái Lan, việc sử dụng dòng thuốc generic cho phép chính phủ cung cấp thuốc miễn phí cho các bệnh nhân có HIV, trong khi chi phí cho thuốc gốc khoảng 450 USD/năm/người. Ngoài ra các bệnh nhân ung thư, viêm khớp, tiểu đường... cũng đang được cứu sống nhờ thuốc generic giá rẻ. |
Thư nêu rõ Roche là chủ sở hữu bằng độc quyền sáng chế số 2641 do Cục Sở hữu trí tuệ VN cấp ngày 11-3-2002, bảo hộ cho sáng chế “Thể tiếp hợp Interferon” đang có hiệu lực tại VN đến ngày
27-5-2017. Là chủ sở hữu bằng sáng chế 2641, Roche có các quyền được Nhà nước bảo hộ độc quyền sử dụng, cho phép và ngăn cấm người khác sử dụng các sáng chế được bảo hộ thuộc bằng sáng chế 2641.
Công ty Roche khẳng định Công ty Nanogen đã có hành vi xâm phạm các quyền của Roche là sử dụng Peginterferon alfa-2a để sản xuất các dược phẩm Pegnano. Vì thế Roche yêu cầu trong vòng 15 ngày (kể từ ngày 15-12) Công ty Nanogen phải chấm dứt ngay việc sản xuất, lưu thông, quảng cáo, chào hàng... các dược phẩm Pegnano.
Roche còn yêu cầu Nanogen phải tiến hành các thủ tục rút bỏ hoặc hủy bỏ số đăng ký (SĐK) lưu hành các dược phẩm Pegnano đã được cấp và vĩnh viễn chấm dứt sử dụng sáng chế “Thể tiếp hợp Interferon” hiện đang được bảo hộ.
Hành trình cấp phép
Nguồn tin của chúng tôi cho biết trước khi các sản phẩm của Nanogen được cấp SĐK lưu hành đã có tranh luận trong nội bộ Bộ Y tế về việc cấp SĐK cho các sản phẩm Pegnano.
Theo hồ sơ, ngày 7-5 Công ty Nanogen nộp hồ sơ đăng ký thuốc tại Cục Quản lý dược (Bộ Y tế) cho các sản phẩm Pegnano nói trên để xin được cấp SĐK lưu hành. Ngày 30-9, ông Trương Quốc Cường - cục trưởng Cục Quản lý dược đồng thời là phó chủ tịch thường trực của hội đồng xét duyệt SĐK thuốc - yêu cầu không cấp SĐK cho ba sản phẩm Pegnano vì văn phòng đại diện Công ty Roche tại VN cho rằng Công ty Nanogen đã vi phạm sở hữu trí tuệ.
Ngày 15-10, Cục Quản lý dược có phiếu trình để cấp SĐK cho 577 loại thuốc (không có ba sản phẩm Pegnano).
Sau khi xem xét hồ sơ, cam kết của Công ty Nanogen, Thứ trưởng Bộ Y tế Cao Minh Quang đã phê đồng ý cấp SĐK cho các sản phẩm này. Tuy nhiên ngày 25-11, trong phiên họp hội đồng xét duyệt thuốc trong nước đợt 124, Cục Quản lý dược tiếp tục không đồng ý cấp SĐK cho các sản phẩm Pegnano vì Roche không đồng ý với giải trình của Công ty Nanogen.
Dù vậy, Thứ trưởng Cao Minh Quang vẫn giữ nguyên quan điểm cấp SĐK cho ba sản phẩm Pegnano vì công ty đã cam kết không vi phạm sở hữu trí tuệ. Ngày 8-12, các sản phẩm Pegnano được cấp SĐK lưu hành.
Không vi phạm
Trao đổi với Tuổi Trẻ về khiếu nại của Công ty Roche, ông Hồ Nhân - giám đốc Công ty Nanogen - khẳng định các sản phẩm Pegnano không vi phạm sở hữu trí tuệ của Roche. Ông Hồ Nhân đã có giải trình chi tiết về mặt khoa học, về mặt sở hữu trí tuệ, về mặt cấu trúc phân tử, việc gắn kết PEG của các sản phẩm.
Theo ông Hồ Nhân, Pegnano là sản phẩm thuộc danh mục sản phẩm công nghệ cao được khuyến khích phát triển và ưu tiên đầu tư của Chính phủ.
Theo ông Nhân, để có các sản phẩm Pegnano đặc trị viêm gan siêu vi C và B, Công ty Nanogen đã đầu tư hơn chín năm qua với quyết tâm sản xuất thuốc đặc trị chuyên khoa tại VN từ nguyên liệu đến thành phẩm với giá cả hợp lý để phục vụ cộng đồng.
Việc sản xuất Pegnano với giá rẻ hơn giá thuốc nước ngoài (khi đến tay người bệnh, tùy theo loại giá thuốc Pegnano sẽ khoảng 1,5-1,9 triệu đồng/liều 180mcg), giúp người dân thuộc các thành phần thu nhập thấp trong xã hội có được thuốc để điều trị, ngăn ngừa lây nhiễm bệnh viêm gan trong cộng đồng. Trong khi chi phí cho một liệu trình điều trị bệnh viêm gan siêu B, C sử dụng sản phẩm độc quyền Pegasys của Công ty Roche là 4,3 triệu đồng/liều 180mcg.
Phần lớn bệnh nhân VN với mức thu nhập bình quân hiện tại không đủ khả năng tài chính để tuân thủ phác đồ điều trị theo giá thuốc độc quyền.
Ông Hồ Nhân cho rằng việc độc quyền thuốc điều trị viêm gan siêu vi với giá thành cao cần phải được xem xét lại theo điều 7 về “giới hạn quyền sở hữu trí tuệ” của Luật sở hữu trí tuệ VN sửa đổi, bổ sung năm 2009. Điều 7 nói rõ trong trường hợp nhằm đảm bảo mục tiêu quốc phòng, an ninh, dân sinh và các lợi ích khác của Nhà nước, xã hội quy định tại luật này, Nhà nước có quyền cấm hoặc hạn chế chủ thể quyền sở hữu trí tuệ thực hiện quyền của mình.
|
Thứ trưởng Bộ Y tế Cao Minh Quang: Chúng tôi cấp số đăng ký đúng luật
Trao đổi với Tuổi Trẻ ngày 20-12, Thứ trưởng Bộ Y tế Cao Minh Quang nói: - Chúng tôi dựa vào điểm 1, 3, 4 trong thông tư 22 năm 2009 quy định việc đăng ký thuốc. Theo quy định này, cơ quan quản lý được quyền cấp số đăng ký cho thuốc Pegnano của Công ty Nanogen. Các điểm 1, 3, 4 trong thông tư 22 đã dẫn quy định rõ: cơ sở đăng ký thuốc phải chịu trách nhiệm về các vấn đề liên quan đến sở hữu trí tuệ của thuốc đăng ký lưu hành. Trường hợp có tranh chấp về sở hữu trí tuệ, bên phản đối phải cung cấp kết luận của cơ quan quản lý nhà nước về sở hữu trí tuệ, hoặc cơ quan có chức năng thực thi quyền sở hữu trí tuệ về hành vi vi phạm. Bộ Y tế sẽ từ chối cấp số đăng ký lưu hành cho thuốc đó nếu có đủ cơ sở để khẳng định thuốc khi được cấp số đăng ký lưu hành vi phạm quyền sở hữu trí tuệ của cá nhân, tổ chức đang được bảo hộ. Trường hợp có tranh chấp về sở hữu trí tuệ sau khi đã cấp số đăng ký lưu hành, cơ quan quản lý nhà nước sẽ xem xét đề nghị của các bên, phán quyết của tòa án hoặc cơ quan quản lý nhà nước về sở hữu trí tuệ, có thể rút số đăng ký lưu hành đã cấp. Như vậy, việc cấp số đăng ký này hoàn toàn đúng luật. * Thưa ông, vậy hiện nay Roche đã chứng minh được vi phạm sở hữu trí tuệ ở thuốc điều trị viêm gan siêu vi này? - Theo tôi biết thì chưa, nhưng ở vai trò của mình, chúng tôi không đi chứng minh việc có vi phạm hay không vì công ty đăng ký thuốc phải chịu trách nhiệm về các vấn đề liên quan đến sở hữu trí tuệ. * Thuốc của hai nhà sản xuất này có gì khác nhau? - Hai thuốc có chất lượng điều trị như nhau, giá thuốc mới cấp chỉ bằng 25% của Roche, chống được độc quyền, sản phẩm mới được cấp lại do công ty 100% VN sản xuất. |
















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận