
TS Marie-Paule Kieny - Ảnh: KEYSTONE
Trong 10 ngày qua, các đơn vị nghiên cứu vắc xin ngừa COVID-19 của Mỹ, Nga, Trung Quốc đã lần lượt công bố kết quả thử nghiệm lâm sàng.
3 loại vắc xin Mỹ và Nga đi đầu
Ngày 9-11, Tập đoàn Pfizer (Mỹ) phát pháo khẳng định theo kết quả ban đầu, vắc xin BNT162b2 hợp tác với Công ty BioNTech (Đức) đạt hiệu quả trên 90%.
Hai ngày sau, đến lượt Nga lên tiếng. Trung tâm Dịch tễ học và vi sinh Gamaleya cùng Quỹ Đầu tư trực tiếp Nga (RDIF) thông báo vắc xin Sputnik-V của Nga đạt hiệu quả bước đầu 92%.
Đến ngày 16-11, Công ty Moderna (Mỹ) loan tin kết quả ban đầu cho thấy vắc xin mRNA-1273 đạt hiệu quả sơ bộ 94,5%.
Ngày 18-11, Pfizer/BioNTech tiếp tục công bố tỉ lệ đạt hiệu quả của BNT162b2 đã lên đến 95% theo kết quả nghiên cứu cuối cùng.
Về phần Trung Quốc, tạp chí y học The Lancet (Anh) hôm 17-11 đã đăng nghiên cứu về vắc xin CoronaVac của Công ty Sinovac Biotech cho thấy CoronaVac an toàn và tạo được phản ứng miễn dịch.
Tuy nhiên, đây là kết quả nghiên cứu của giai đoạn 1 và giai đoạn 2 chứ không phải ở giai đoạn 3 như 3 loại vắc xin của Mỹ và Nga.
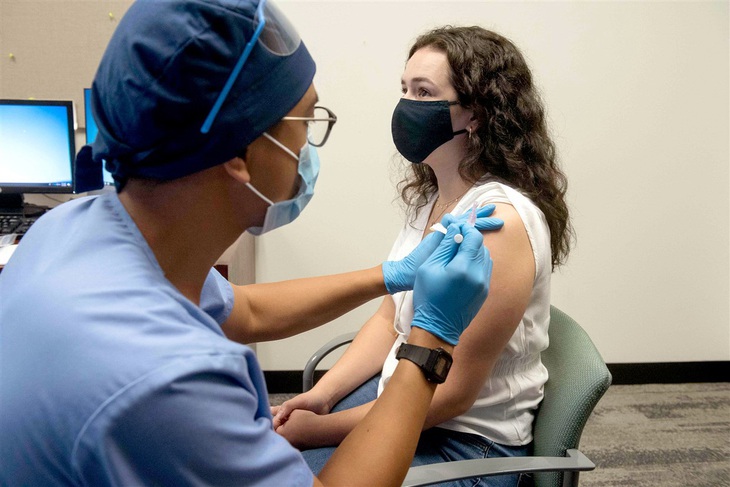
Người tình nguyện được tiêm vắc xin mRNA-1273 của Moberna ở Detroit ngày 5-8-2020 - Ảnh: AFP
Hai câu hỏi cần giải đáp
TS Marie-Paule Kieny chuyên về virus học và tiêm chủng học đang giữ chức chủ tịch Ủy ban Khoa học về vắc xin COVID-19 thuộc Bộ Y tế Pháp.
Bà là giám đốc nghiên cứu của Viện Nghiên cứu sức khỏe và y học quốc gia Pháp (INSERM), nguyên trợ lý tổng giám đốc Tổ chức Y tế thế giới (WHO) từ năm 2011-2017.
Trả lời trang web The Conversation (Pháp), bà nhận xét: "Cộng đồng của chúng tôi không hình dung tỉ lệ lớn như thế đối với các loại vắc xin ngừa COVID-19 đầu tiên. Đây là thông tin rất tốt, giúp chúng ta lạc quan nhìn về tương lai. Dù vậy, chúng ta vẫn chưa biết một số thông số rất quan trọng".
Theo bà, có hai vấn đề chưa rõ. Một là tính hiệu quả lâu dài. Vắc xin phải ngăn ngừa bệnh tật trong thời gian dài và có thể là suốt đời như vắc xin ngừa bệnh sốt vàng.
Dù vậy, đến nay chưa thể nói trước vắc xin ngừa COVID-19 bảo vệ bao lâu, sau 3, 6, 12 tháng hoặc dài hơn.
Vấn đề thứ hai rất quan trọng: vắc xin có bảo vệ tốt người cao tuổi hay không?
TS Marie-Paule Kieny giải thích: "Các thể nặng và tử vong xảy ra chủ yếu trong thành phần dân số này và phản ứng miễn dịch cũng thường kém hiệu quả hơn. Kết quả ban đầu do Pfizer và Moderna công bố không nêu rõ khác biệt theo lứa tuổi.
Dữ liệu này cần được xác thực. Do đó, chúng tôi đang chờ công bố kết quả nghiên cứu đầy đủ trên các tạp chí có bình duyệt để có thể phân tích chi tiết dữ liệu về tính hiệu quả và độ an toàn".
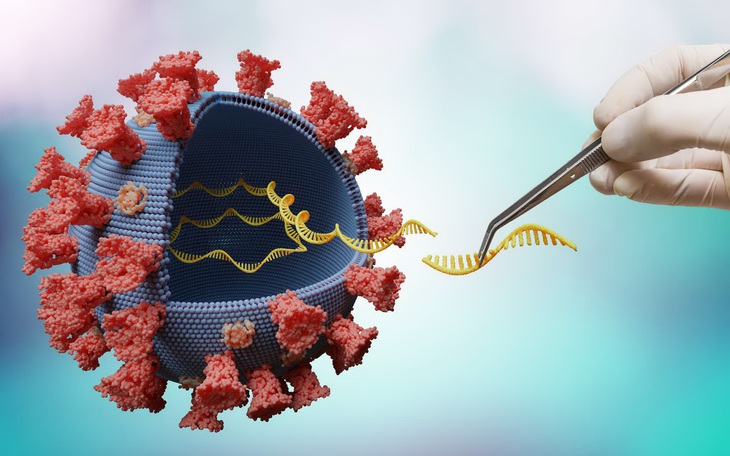
Moderna và Pfizer cùng sử dụng công nghệ ARN thông tin để sản xuất vắc xin - Ảnh: futura-sciences.com
Công nghệ mới ARN thông tin là gì?
* Vắc xin của Pfizer và Moderna dựa trên công nghệ mới vắc xin ARN. Công nghệ này có các đặc điểm cụ thể gì?
TS Marie-Paule Kieny: Hầu hết các loại vắc xin sử dụng virus đã bị giết bằng hóa chất, virus hoặc một bộ phận nhỏ virus đã giảm độc lực, do đó virus không còn mang mầm bệnh để sinh sản. Mục đích nhằm tạo phản ứng miễn dịch hiệu quả nếu có tiếp xúc với virus thật.
Công nghệ vắc xin ARN thì khác (ARN thông tin - hay mRNA là ARN đã mã hóa và mang thông tin từ ADN tới vị trí tổng hợp protein). Công nghệ này nhằm tiêm vật liệu di truyền của virus để các tế bào sản sinh một hoặc nhiều protein virus, sau đó protein virus sẽ được hệ miễn dịch của chúng ta nhận dạng.
Nhược điểm của công nghệ ARN thông tin là bản thân phân tử ARN rất mỏng manh, vì thế Pfizer khuyến cáo nên bảo quản vắc xin ở nhiệt độ -70°C…
Moderna đã phát triển thành công vắc xin ổn định nhiều tháng ở nhiệt độ -20°C và thậm chí 30 ngày ở nhiệt độ tủ lạnh (4°C) hoặc thậm chí 12 tiếng trong nhiệt độ phòng.

Phòng thí nghiệm vắc xin ngừa COVID-19 của Công ty BioNTech ở Đức - Ảnh: BIONTECH
Dữ liệu về độ an toàn không nhiều
* Chúng ta biết gì về độ an toàn của vắc xin?
TS Marie-Paule Kieny: Hiện thời dữ liệu về độ an toàn không nhiều. Chúng ta đã biết khả năng gây ra phản ứng (reactogenicity) hoặc cách cơ thể phản ứng khi tiêm vắc xin là nhức đầu, đau, sưng ở cánh tay hoặc buồn nôn.
Chúng tôi quan sát thấy vắc xin ARN dễ gây phản ứng hơn các vắc xin khác như vắc xin chống cúm, điều này vẫn chấp nhận được.
Điều chúng ta chưa biết là các tác dụng phụ lâu dài hơn sẽ xuất hiện khi số người được chủng ngừa tăng lên theo thời gian.
Các cơ quan y tế rất chú ý đến vấn đề này. Ví dụ Cơ quan Quản lý thực phẩm và dược phẩm Mỹ (FDA) đã yêu cầu các công ty cung cấp dữ liệu tối thiểu liên quan đến 50% nhóm được tiêm chủng, tức khoảng 10.000 người tình nguyện với thời gian theo dõi tối thiểu hai tháng.
Có thể có giấy phép lưu hành vào tháng 12-2020
* Vậy khi nào vắc xin được đưa ra thị trường?
TS Marie-Paule Kieny: Các cơ quan y tế phải bật đèn xanh. BioNTech/Pfizer và Moderna sẽ phải cung cấp cho FDA dữ liệu về an toàn vào cuối tháng 11-2020.
Nếu không có vấn đề gì trục trặc, giấy phép lưu hành sẽ được cấp vào tháng 12-2020.
Đối với châu Âu, cơ quan tương đương với FDA là Cơ quan Quản lý dược phẩm châu Âu (EMA).
Thủ tục và thời gian cấp phép cũng tương tự. Sau khi có giấy phép, các nhà sản xuất mới có thể cung cấp số lượng lớn vắc xin.

















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận